Reaksi Diels-Alder
Diels-Alder merupakan
salah satu reaksi yang paling penting dalam sintesis disebabkan reksi berguna untuk membuat dua
ikatan C-C dalam satu langkah dan karena
bersifat regio dan stereoselektif. Ia merupakan siklo addisi perisiklik antara diena
tearkonjugasi (1) yang menjalani jenis adisi 1,4. Diena harus memiliki apa yang disebut dengan konformasi s-cis untuk melangsungkan suatu reaksi diels - alder dan alkena terkonjugasi (2) (dienofil), membentuk sikloheksena.
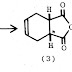
contoh lain yang paling sederhana(masih menghasilkan rendemen yang rendah):
Reaksi ini merupakan contoh reaksi sikloadisi, yaitu adisi
yang menghasilkan produk siklik. Sikloadisi ini, yang mengonversi tiga ikatan π
menjadi dua ikatan σ dan satu ikatan π baru, dinamakan reaksi Diels-Alder,
berdasarkan nama penemunya, yaitu Otto Diels dan Kurt Alder. Reaksi ini begitu
berguna untuk membuat senyawa siklik sehingga mereka memperoleh Hadiah Nobel
dalam bidang kimia pada tahun 1950. Sebagaimana halnya dengan hidroborasi,
reaksi ini berlangsung serempak. Semua pemutusan ikatan dan pembuatan ikatan
berlangsung pada saat yang sama.
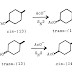
Ketika diena dan dienofil bereaksi dalam reaksi Diels-Alder, terbentuklah sebuah senyawa stereokimia karena kedua reaktan tersebut saling mendekat dari dua arah yang berbeda. Jenis pendekatan ini memungkinkan awan elektron dari dua komponen tumpang tindih dan membentuk ikatan produk yang lebih stabil. Bentuk stereokimia dari molekul produk ada 2 jenis yaitu : dienofil yang mensubstitusi berada pada posisi berlawanan dengan diena (cis) akan menghasilkan produk adisi “endo” dan dienofil yang mensubstitusi berada pada posisi sepihak dengan diena (trans) akan menghasilkan produk adisi “exo".
Ketika diena dan dienofil bereaksi dalam reaksi Diels-Alder, terbentuklah sebuah senyawa stereokimia karena kedua reaktan tersebut saling mendekat dari dua arah yang berbeda. Jenis pendekatan ini memungkinkan awan elektron dari dua komponen tumpang tindih dan membentuk ikatan produk yang lebih stabil. Bentuk stereokimia dari molekul produk ada 2 jenis yaitu : dienofil yang mensubstitusi berada pada posisi berlawanan dengan diena (cis) akan menghasilkan produk adisi “endo” dan dienofil yang mensubstitusi berada pada posisi sepihak dengan diena (trans) akan menghasilkan produk adisi “exo".
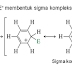
Pada reaksi perisiklik, diskoneksi yang bersangkutan sering ditemukan dengan membuat
mekanisme reaksi balik ketika ingin membuat sikloheksena (4) dengan paling
sedikit 1 gugus penarik elektron (Z) pada tempat yang jauh dari cincin, buat
tiga anak panah sekitar cincin ikatan rangkap.
Salah satu contoh reaksi perisiklik adalah pada senyawa (6) yaitu 1-(3-methylcyclohex-3-en-1-yl)ethanone
dengan reaksi Diels-Alder menyebabkan senyawa berada dalam posisi orto
dan para akan tetapi memberikan produk meta seperti (7) sebagai ganti. Keton (6) adalah senyawa karbonil ɣ, δ-yang tidak jenuh dan dengan demikian dapat dibuat dengan penataan ulang
Claisen Cope. Diskoneksi adalah sukar untuk diikuti, tetapi bilangan
pada (8) dan (9) akan membantu.
Struktur (9) sangat dekat dengan dimer Diels-Alder (10).
dari metil vinil 'keton dan reaksi Wittig mengkoneksi mereka.
Dimerisasi yang memberikan (10) biasanya suatu gangguan, tetapi ia membuat (10) cepat tersedia. Penataan
ulang berjalan dari (9) ke (16) disebabkan gugus karbonil terbentuk atas tanggungan ikatan rangkap C=C yang kurang stabil.
DAFTAR PUSTAKA
Hart, H., L. E. Craine dan D. J. Hart. 2003. Kimia Organik. Jakarta: Erlangga.
Warren, S. 1994. Sintesis Organik Pendekatan Diskoneksi. Yogyakarta: UGM-Press.
PERTANYAAN:
1. Pada reaksi sikloadisi 2 isopren (2-metil-1,3-butadiena) diketahui sebagai starting material pada sintesis limonena, bagaimana hal ini dapat terjadi berdasarkan aturan diena dan dienofil?
2. Pada reaksi pembentukan sikloheksana diatas terbentuk melalui starting material yang sederhana pada dienofilnya (etilena) yang dinyatakan menghasilkan rendemen tidak baik , bagaimana pengaruh dienofil dapat dengan nyata mempengaruhi hasil sintesis yang dilakukan?











Tidak ada komentar:
Posting Komentar